含まれる食塩(g) = 食塩水(g) × 濃度(%) 100 はじめの食塩水の濃度をx%とする。 x%の食塩水700gに含まれる食塩は 700× x 100 =7x(g) 水を300g蒸発させると食塩水の質量は=400gとなる。 7%の食塩水400gに含まれる食塩は 400× 7 100 =28g 濃度(%) x 0(水) 7 食塩水(g) 400 含ま1)水100gにNaClを25g溶かしたときの重量%濃度は? (答え) % 2)5%の食塩水0g中に含まれる食塩は何g? (答え) 10g ※この例題の解説(計算式)は こちらへ 溶液の重量(体積)100万(million)に対する溶質の重量(体積)を表したもの(100万分の1濃度)解答:100g 12. 食塩15gと水285gを混ぜ、火にかけていきました。 (1)すべて混ざり合うと濃さは何%ですか。 (2)火をかけ続け、水が何gか蒸発したので、濃さを調べたところ、10%でした。 水は何g蒸発しましたか。 解説: (1)食塩水の公式から 15÷(15+285)=005→5%。

我的記事簿 Scr Pfd 計算過程 1 8
濃度 計算 問題 高校
濃度 計算 問題 高校-計算した後は,その量を質量とか体積とかに変換しなければならない. それでは以下の(10)から(12)を計算してみよう. (10) 3 mol L1の塩化ナトリウム水溶液500 mLを調製するために必要な塩化 ナトリウムは何molか計算せよ.それは何gか計算せよ.NaCl=585と せよ.問題2 5%グルコース500ml輸液バックに50%ブドウ糖液mlを3本混合しました。 この混合液にはブドウ糖は何g入っていますか。 また、この液のブドウ糖の濃度は何%ですか。 計算では1の位を四捨五入してください。 (図:50%ブドウ糖ml)




小學數學寒假自補 濃度問題口訣及解題方法附經典應用題及答案 每日頭條
· 將 B cup 液體倒入 A cup , 變成 A cup , 水量為 A B , 內容物為 02A 006B , 而濃度為 12% 所以 (02A006B) / (AB) = 012 得知 B = A 的 4 / 3 所以請由 B cup 倒 A cup 的 4/3 份量到 A cup 回應 6 分享 檢舉 2 kradark iT邦好手 1 級 ‧ 17モル濃度を求める問題では、ほとんどの場合、ここがスタートになります。 質量パーセント濃度〔%〕=(溶質の質量〔g〕/水溶液の質量〔g〕)×100 次に、密度と質量パーセント濃度を使って、 溶質の質量 を求めましょう。Mixi看護師国家試験 薬液の計算式を教えて下さい 来春10年に国試を受ける予定で、医学書院の「10年版 系統別 看護師国家試験問題 回答と解説」と言う電話帳サイズの問題集で勉強をはじめました。166ページの問題8がどうも理解出来なくて困ってい
· この問題も問題1と同じ考え方で解けます。 食塩水の濃度とは、ある食塩水を100gに相当させた場合、その中にどれくらいの食塩が溶けているかを表す数(割合)です。 濃度が10%の食塩水とは、食塩水100g相当の中に食塩10gが溶けている食塩水です。01 · 質量パーセント濃度の計算問題集基本編 科学者たちは、質量パーセント濃度という基準をつくり、世界を発展させたことは学びましたよね。 具体的にいえば、 「この溶液が100gあったとき、溶質は何gあるのか? 」 を示す指標です。 質量C 濃度の計算 食塩水などの溶液の濃度の問題を解くときに重要なポイントは「溶液=溶質+溶媒」と いうことです。溶質(溶けている物質)の量に着目することが特に重要です。 濃度、溶質の量、溶媒の量は次の式から求めます。
· 濃度は、割合を100倍した百分率 (%)で表されている ので、 割合を求めるには濃度を100で割る必要がある のです。 この問題では濃度が8%なので、 割合は8を100で割った008 になりま溶液 = 溶媒 溶質 なので 質量パーセント濃度 = 溶質 (g) 溶質 (g) 溶媒 (g) ×100 濃度を求めるときに分母は溶液である。 水は溶媒なので、分母は砂糖水全体の質量になる。 例水80gに砂糖gを溶かして砂糖水をつくる。 この砂糖水の質量パーセント濃度を求める。 質量パーセント濃度 = 溶質 (g) 溶質 (g) 溶媒 (g) ×100 なので 式 質量パーセント濃度 = · 一般常識「濃度算」の練習問題(高校生対応) 投稿日:19年6月14日 更新日:19年6月16日 <例題1> 食塩40gを1gの水に溶かすと何%の食塩水ができるか。 ≫ 例題1の解答・解説を見る 答え:25% 食塩の濃度は次の式で求めます。 濃度(%)=食塩の量÷食塩水の量×100 分数にすると ここで注意したいのは、食塩水は「食塩+水」であるということ。




濃度稀釋計算問題 濃度稀釋計算




3种方法来计算溶液浓度
1402 · 濃度の違う食塩水を混ぜる問題の解き方1計算問題付 それでは、濃度算に関する練習問題を解いていきましょう。 ・例題1 濃度が5%の食塩水0gと、濃度が10%の食塩水300gを混ぜた際の濃度は何パーセントになるでしょうか。 ・解答1 · 塩10gと水90mlが混ざり合ってできた食塩水100mlの濃度は何%であるかの計算をします。 溶解全体量:100ml 濃度:解答 溶質量:10g 100ml×濃度=10g この時に両辺に「100」で割ると 100ml÷100×濃度=10g÷100 濃度=01 となります。 これで濃度が「01」であることがわかり12. 食塩15gと水285gを混ぜ、火にかけていきました。 (1)すべて混ざり合うと濃さは何%ですか。 (2)火をかけ続け、水が何gか蒸発したので、濃さを調べたところ、10%でした。 水は何g蒸発しましたか。 13. 4%の食塩水300gに食塩を2g入れて、火にかけて、水を蒸発させたところ、 5%の食塩水になりました。 水は何g蒸発しましたか。



高一化学物质的量浓度溶液的配置 米粒分享网 Mi6fx Com




高中化学考点归纳6 一定物质的量浓度溶液的配制与计算 王羽课堂
濃度のわからない食塩水MとNがそれぞれ800gずつある。 Mから300gとNから500gを取り出してこれらを混ぜると8%の食塩水になり、残りの食塩水をすべて混ぜてさらに、水を160g加えると10%の食塩水ができる。 MとNの濃度をそれぞれ求めなさい。 式 答濃度の変換問題は,質量パーセント濃度% ⇔ モル濃度mol/L の変換が頻出となる。 Ⅰ質量パーセント濃度に関する問題タイプ Ⅱモル濃度に関する問題タイプ ・質量パーセント濃度:溶液中に溶けている溶質の質量を百分率で表した濃度。溶液100gあたりの 溶質の質量g。 ・モル濃度:溶液1L中に溶けている溶質の物質量molで表した濃度。 · 濃度計算のコツ~まずはこのやり方を覚えよう~ (例)10%塩化ナトリウム水溶液を用いて、02%塩化ナトリウム溶液を500ml作るために必要な10%塩化ナトリウム水溶液量は何mlか。 ※この問題の場合、原液は10%塩化ナトリウム水溶液ということになります。




小學數學寒假自補 濃度問題口訣及解題方法附經典應用題及答案 每日頭條



高中化學之由水電離出的氫離子和氫氧根離子濃度計算問題解析 愛經驗
· 濃度の問題 中学受験でよく出題される食塩水の濃度の問題です。 濃度は割合の考え方が身につけて基本的な問題はすぐに解けるように練習してください。 食塩水と食塩水を混ぜる問題は 面積図 で考えることが多くなります。 また比を使う考え方も利用濃度を計算する問題 2組の入口へ 説明へGO 1 水酸化ナトリウムの結晶gを水80gに溶解させ、水酸化ナトリウム水溶液を作る。この水溶液の密度を12g/cm 3 とするとき、以の濃度を求めよ。 (原子量H=10,O=16,Na=23) 1,質量パーセント濃度 2,モル濃度第Ⅱ章 栄養士のための割合を使った計算問題 第Ⅰ章で、割合計算の基礎を学んできましたが、割合の基礎が分かれば、栄養士に必要な計 算問題は、少しの応用でできるようになります。 第1節 三大栄養素に関する計算問題 例題1




濃度稀釋計算問題 濃度稀釋計算




摩尔浓度的计算
モル濃度は 13 で学んだ通り、モル濃度( mol / L )= 溶質の物質量( mol )÷ 溶液の体積( L )で導きます。 また溶液の体積は、次のように変換することもできることも使って計算しましょう。 溶液の体積( L )= 溶液の体積( mL )÷ 1000質量パーセント濃度〔%〕= (溶質の質量〔g〕/溶液の質量〔g〕)×100 (1)は、質量パーセント濃度を求める問題です。 質量パーセント濃度の求め方を覚えていますか? 質量パーセント濃度〔%〕= (溶質の質量〔g〕/溶液の質量〔g〕)×100 この式に、溶液の質量0g、溶質の質量4gを当てはめましょう。 (4g/0g)×100=2% よって、答えは 2% です。濃度算(食塩水問題)の文章問題計算ドリル/問題集 管理人 11月 2, 18 小学校算数の割合に関する文章問題として代表的なもののひとつ「濃度算」。 これの問題集です。 基本の公式を抑えるための問題と、文章問題を用意しました。 問題をランダムで生成することができ、答えの表示・非表示も切り替えられます。 印刷してご活用ください。 文章問題は




モル計算 濃度計算などの問題 解説 レベルa2 ともよし塾 受験と科学の解説授業




國一上三段段衝精選類46 濃度問題asepx凱爺數學 Youtube
0901 · 質量パーセント濃度の計算問題集基本編 科学者たちは、質量パーセント濃度という基準をつくり、世界を発展させたことは学びましたよね。 具体的にいえば、「この溶液が100gあったとき、溶質は何gあるのか? 」を示す指標です。 実はこのパーセント (%)、あまりにも便利な menonnetwork 0102 シンプルなかけ算や割り算があるだけで簡単な質量ここでは体積モル濃度(以後単にモル濃度と表します。)について計算問題を解いて行きます。 モル濃度計算でやっておきたい単位換算と公式の確認 モル濃度は \(\mathrm{mol/L}\) が単位なので溶液が \(\mathrm{L}\) 単位であれば問題はないのですが、濃度計算の問題です。 (公務員 数的推理) こちらの問題を方程式で解こうとするとどのような式になりますか? 濃度%の食塩水0グラムに対して、次の1〜4の手順を行っ



科学网 测的水质氯化物 为啥监测报告中是氯离子 霍小鹏的博文




我的記事簿 Scr Pfd 計算過程 1 8
1 (1)答8% 解説 質量パーセント濃度 = 溶質 (g) 溶液 (g) ×100より 250 ×100=8 (2)答 250g % 解説 ① 砂糖水 (溶液) = 砂糖 (溶質)水 (溶媒) より 500=250 ② 質量パーセント濃度 = 溶質 (g) 溶液 (g) ×100より 50 250 ×100= (3)答375% 解説 砂糖水 (溶液) = 砂糖 (溶質)水 (溶媒) より 砂糖水の質量は=160g 質量パーセント濃度 = 溶質 (g) 溶液 (g) ×100よ化学 モル濃度 計算問題 化学の計算問題が参考書等買ってやってみたのですがわかりません。 どのかたかわかる方お願いします。 質量パーセント濃度96.0%、密度1.84g/cm3 の濃硫酸を水で薄 質濃度計算 質量パーセント濃度を求めよ。 (割り切れない場合は小数第1位を四捨五入して整数で答えよ) 0gの水溶液の中に、溶質が30gが溶けている場合。 水460gに溶質40gを溶かした水溶液。 150gの水溶液のうち、100gが溶媒の場合。 次の問いに答えよ。 濃度8%の水溶液が600gある。 この水溶液中に溶けている溶質の質量を求めよ。 。




化学 转化率问题 化学浓度商怎么计算 桃丽网
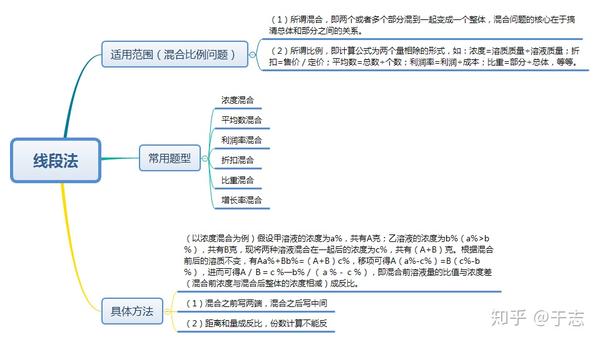



数量关系 核心方法 线段法 知乎
· 食塩水の濃度の計算ドリル 概要 食塩水の濃度についての文章題です。 計算自体は易しくなるように作りましたが、問題が多いので、てんびん図や面積図を習ってから取り組むのが理想的物質 問題 チェックテスト いろいろな物質 密度計算 水溶液 濃度溶解度計算 気体 状態変化 基本問題 いろいろな物質 密度計算問題 身の回りの物質 気体1 気体2 気体3 水溶液の性質 水溶液の性質2 濃度計算問題 アンモニアの噴水実験 メスシリンダーの使いこれは第1回の問題演習より 難易度が上がっています。 第1回の問題演習はこちら、 「濃度計算問題の問題演習①合法カンニングペーパーの使い方」 前回は、1発合法カンペを使えば、 終了の問題でした。 しかし、今回は、それだけでは 解けません。



高一化学题 关于转化率计算 化学平衡的问题




食塩水問題 濃度算 の2つの解き方とポイントを図で解説 数学fun



化学平衡常数kp的计算基础内容 哔哩哔哩 つロ干杯 Bilibili




公务员考试 行测涉及的计算公式都在这里了 教育频道 手机搜狐




1 4觀念09溶液的稀釋與混合 Youtube




これで分かる モル濃度計算の解き方 大村升次郎 大村升次郎 本 通販 Amazon




溶液的稀释公式 溶液稀释定律公式是什么 三人行教育网 Www 3rxing Org



行测80分必备 数学运算经典题型全集下载 Word模板 爱问共享资料



普通化學濃度計算問題 考試板 Dcard




高校化学基礎 濃度の計算 練習編 映像授業のtry It トライイット




日本东电拟排放核污水前不测放射性物质浓度 日网友批 想敷衍了事




实用 精油浓度计算表 请收藏 知乎
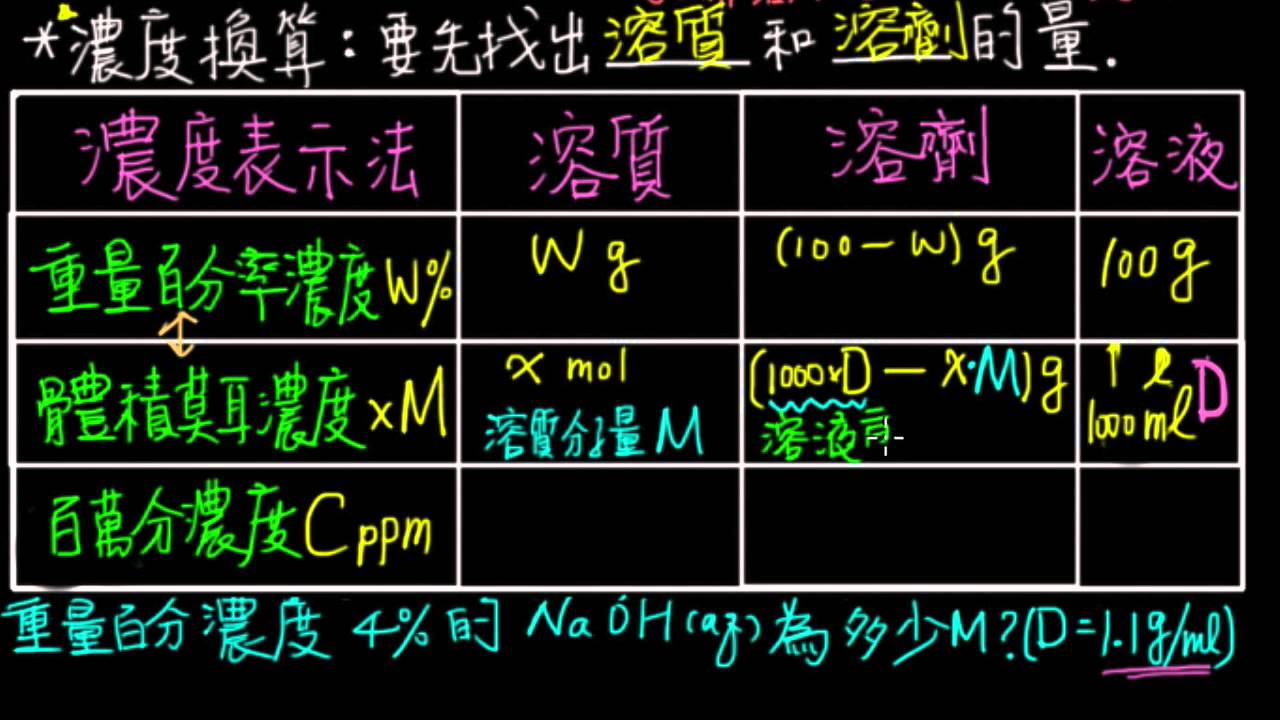



1 4觀念10溶液的濃度換算 Youtube



如何计算糖与糖水的质量比 三道题帮你解决 浓度问题




質量パーセント濃度の計算問題集 基本編 Menon Network



Spi3 問題無料 言語非言語テストセンターwebテスト就職一般常識濃度計算 安卓下載 安卓版apk 免費下載



浓度计算公式有哪些 高三网



公考行測秒殺技巧 濃度問題解題方法 愛經驗
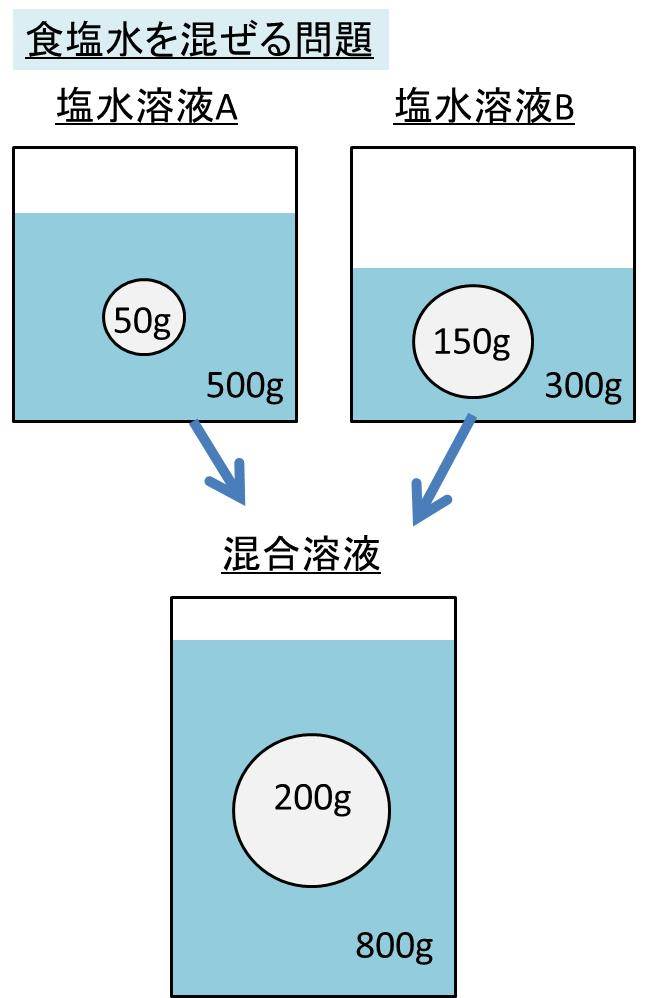



Spi 異なる濃度の食塩水を混ぜる問題の計算方法 濃度算



溶液浓缩计算问题 腾讯视频




濃度算 食塩水問題 の文章問題 計算ドリル 問題集 数学fun



Http Www Whxb Pku Edu Cn Dxhx Cn Article Downloadarticlefile Do Attachtype Pdf Id




如何计算初始浓度 科学 21



溶液加水稀释浓度计算 西瓜视频搜索




濃度與配比問題 每日頭條



高一化学物质的量浓度的计算 第五题 信息阅读欣赏 信息村 K0w0m Com




3种方法来计算溶液浓度




體積莫耳濃度的文章和評論 痞客邦




看護学科の化学講義 16 溶液濃度計算問題演習 Life Chemistry




小学数学浓度问题 抓住两个量 就没有难度了 Tnaot




改訂版 大学入試 ゼロからはじめる 化学計算問題の解き方 Amazon Com Books




濃度與配比問題 每日頭條



Mg G Ppm Zonealarm Results




小學數學寒假自補 濃度問題口訣及解題方法附經典應用題及答案 每日頭條



两道题搞懂a Level化学kpc题型 翰林国际教育



高中化学专题知识讲解 过量计算问题归类解析 高中化学 学习资料大全 免费学习资源下载




滴定定义 曲线 摩尔浓度方程等




小学数学浓度问题 抓住两个量 就没有难度了 Tnaot




第二节定量分析方法特点 一 容量分析法的特点容量分析法是将已知浓度 的滴定液由滴定管滴加到待测药物的溶液中 直到所加滴定液与被测药物按化学计量反应完全为止 然后根据滴定液的浓度和消耗的体积 就可计算出被测药物的含量 Ppt Download




Pdf 濃度の計算ドリル45題 中学理科ポイントまとめと整理 オンラインショップ




モノマナビ研究所
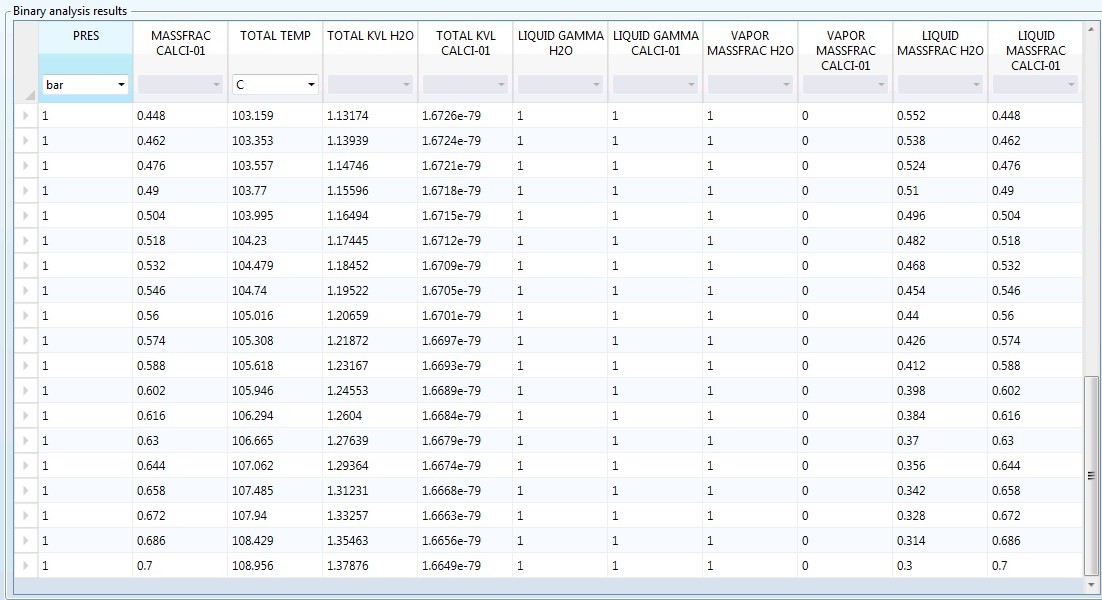



利用apsen计算氯化钙 Cacl2 水溶液沸点的问题利用aspen计算氯化钙水溶液的沸点 在1bar 浓度 70 下 采用物性方法为elecnrtl 经过模拟计算出沸点为109度 这和工具书上查出来的175度相差甚远 不知道是什么原因是物性




濃度を求める問題 プロ家庭教師あゆこ先生の勉強応援ブログ




粉笔网




質量パーセント濃度の計算問題集 応用編 Menon Network




濃度計算公式濃度的計算方式 Doreff



中1理科 濃度の計算特訓 混ぜ合わせの濃度計算まで Pikuu



浓度的计算公式浓度计算公式数学 麦税尼网




溶液配制神器 摩尔浓度自动计算excel工具 艾美捷奉献 企业动态 丁香通



氯化钠溶液在生产 生活中都有广泛的用途 现配置1 L 0 2 Mol L Nacl溶液 请回答问题 高中一年级 化学试题 配制一定物质的量浓度 的溶液考点 好技网




中1理科 濃度の計算特訓 混ぜ合わせの濃度計算まで Pikuu




Vymgi9gtr Hrum



これで理科マスター 質量パーセント濃度を計算する5つの問題 Qikeru 学びを楽しくわかりやすく



看護学科の化学講義 16 溶液濃度計算問題演習 Life Chemistry




2 1認識電解質2 2 溶液與離子2 3 常見的酸與鹼2 4 酸鹼的濃度2 5 酸與鹼的反應 Ppt Download




浓度问题 知乎




Spi3 問題無料 言語非言語テストセンターwebテスト就職一般常識濃度計算 安卓下載 安卓版apk 免費下載




高校化学基礎 モル濃度の計算 練習編 映像授業のtry It トライイット



数学运算 计算问题之算式计算 91up快学堂



如何计算糖与糖水的质量比 三道题帮你解决 浓度问题




Spi3 問題無料 言語非言語テストセンターwebテスト就職一般常識濃度計算 安卓下載 安卓版apk 免費下載



浓度的计算公式浓度计算公式数学 麦税尼网



求助 关于营养液山崎配方中浓度计算问题 农林 小木虫 学术科研互动社区




基礎 容積莫耳濃度 均一教育平台



浓度的计算公式浓度计算公式数学 麦税尼网



配制溶液浓度计算公式 西瓜视频搜索



速解丨数量关系中的浓度问题 应用



物质的量浓度2 2 备课吧



高一化学 物质的量浓度稀释问题相关计算 哔哩哔哩 つロ干杯 Bilibili




高中化学考点归纳6 一定物质的量浓度溶液的配制与计算 王羽课堂



六年级奥数举一反三小升初数学思维备战新初一分班考试第18讲面积计算 一 知识 名师课堂 爱奇艺




3种方法来计算溶液浓度




請教此題的第一小題答案畫線的部分讓我感到困惑 Clear



摩尔浓度计算 西瓜视频搜索




国考招警行测数量关系指导 用 溶质 突破浓度问题 中公警法考试网



Qck0d2a9as2853cudbqy0lc6cfz4a0e7e Xyz Theory Mol L




國一上三段段衝精選題46 濃度問題asepx凱爺數學 Youtube




六年级奥林匹克数学第17讲浓度问题下载 Word模板 爱问共享资料



食鹽水濃度計算題 數學板 Dcard



溶液浓缩计算问题 腾讯视频




怎么算出体积摩尔浓度 Molarity 生活百科




4种计算摩尔浓度的方法 提示 21



11届化学高考一轮复习教学案第05讲物质的量浓度下载 Word模板 爱问共享资料




中1理科 濃度の計算特訓 混ぜ合わせの濃度計算まで Pikuu




浓度稀释的计算公式 搜狗搜索




用例子理解排列组合及基本公式如何计算 百科 图解吧


